号外,据CBC报道,加拿大总理杜鲁多在今天上午的讲话中称,最少25万加拿大人在今年内(3周内)接种辉瑞新冠疫苗。
加拿大接收24.9万支新冠疫苗!下周就到安省!
今天,加拿大总理杜鲁多宣布,加拿大会在12月份签收多达24.9万支疫苗。这批疫苗主要用于长期护理院的居民和在那里的工作人员。
虽然疫苗仍然在加拿大卫生部的批准之中,但杜鲁多表示,首批疫苗将在下周交付分发,而且其余批次将会在2021年陆续到达。
杜鲁多说:“我们正在面临着国家历史上最大规模的免疫接种。预计将要数月才能完成。”
“这不是一项小任务,因此我们有一个清晰的计划。我们的政府会通过国家操作中心,一直与各个省份和地区合作,以确保我们可以在批准和交付疫苗后,立即分发。”
与此同时,安省省长福特今早表示,加拿大接收的这批疫苗,最早将于下周在安省分发。福特说:“安省正在准备在疫苗到达后,立即分发这批非常少量的疫苗。”
“要让每一个人获得疫苗,任重而道远。我必须重申一次,我们距离实现大规模免疫所需的数百万支疫苗还很远。”
目前,加拿大已经与辉瑞公司签署了2000万支疫苗的订购协议,首批400万支疫苗将在2021年前3个月送达。该协议还允许加拿大有选择权,继续购买额外5600万支疫苗。辉瑞疫苗需要接种2支才能有效。
加拿大卫生部对辉瑞疫苗的审查正在进行,但是很快就会完成。卫生部首席医学顾问Dr. Supriya Sharma表示,她的部门可能最早在本周就会批准辉瑞疫苗。该时间表与美国监管机构的疫苗批准计划大致相同。
昨天,辉瑞疫苗的合作方德国BioNTech公司的首席业务和商务官Sean Marett表示:“我们已经准备好疫苗,一旦加拿大批准,24小时内就可以发货!”
同时,加拿大公共卫生局(PHAC)的物流和运营副总监(VP)Dany Fortin少将说:“我们预计,在明年1月份会有源源不断的疫苗,包括辉瑞疫苗和其他可用疫苗。然后,它们将会在规定的时间范围内,被一波接着一波地分发。”
Fortin少将对记者表示,他的计划是基于在新年之初收到疫苗的期望。“我目前能告诉你的是,我们希望在1月份收到疫苗,并且我们希望在那个时间范围内尽快收到它们,并且能够连续多次交付。”
他说:“我们的计划会从1月份开始执行。对我们而言,临近这个日期才开始准备,并不是一个明智的军事计划。因此,我们其实在12月中旬就会准备就绪。”
也就是说,就算是现在疫苗提前来了,加拿大也能立即行动!不过,近期有民调显示,有相当一部分的加拿大人表示他们将完全拒绝接种新冠疫苗,或者是等待一段时间后再接种。杜鲁多说,他希望加拿大人可以放心,加拿大的监管机构只会批准有效的产品,不会急于求成。
加拿大疫苗一点都不晚!和美国一样,仅次于英国。
Moderna公司创始人和主席Noubar Afeyan上周日接受加拿大CBC采访时称, 加拿大在获分配疫苗方面并不落后。
Moderna公司生产的新冠病毒疫苗 , 据说有效率可达94.5% 。
Noubar Afeyan称,这是因为加拿大是预订Moderna新冠疫苗的首批国家。
所以加拿大可以保证获得该公司的第一批(initial batch)出产疫苗的一部分。
Afeyan称,那些在疫苗效果还不知道的时候,就出钱的人,肯定可以获得相应的份额(出钱多少就分多少)。
Afeyan表示,不管后面发生什么,也改变不了这个事实。
高盛:加拿大和美国在明年4月前将有50%的人接种疫苗
另据高盛的最新预计,英国在明年3月之前将有50%的人接种疫苗,加拿大和美国在明年4月前将有50%的人接种疫苗
欧盟、澳大利亚和日本的接种人数可能会在5月份达到50% 。
民调指75%多市市民愿意接种新冠疫苗(图)
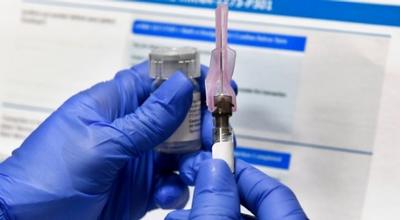
据多伦多市公共卫生局委托Ipsos Reid公司所做的民意调查显示,有75%的市民愿意接种新冠疫苗,超过世卫达到全民免疫的比例要求。
调查亦指出,有40%表示一定会接种,有33%称则称可能会。
另外,16%的受访者则表示不会或可能不会接种疫苗。另外有11%表示不知道。
调查访问了1201名市民。
审批辉瑞疫苗采弹性处理 允药厂「滚动报告」省时间(图)
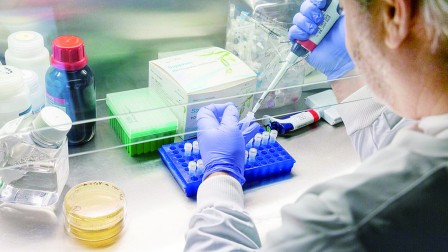
联邦卫生部正在审批辉瑞药厂等的疫苗,今次的审批过程增加了弹性。
加拿大联邦卫生部正在审批辉瑞药厂等的疫苗,今次的审批过程增加了弹性,允许药厂从试制阶段的一开始,就「滚动报告」各种数据,而不是惯常的在完成所有试验之后,再把全部数据、资料呈报。这样可节省许多时间。卫生部首席医学顾问沙玛(Supriya Shama)说,滚动报告的情况下,所有必须做的试验、所有必须报告的数据,一样都不可缺少。因此在节省时间的同时,并不影响疫苗的安全性和功效。
疫苗厂商的一次性呈交的报告有数千页之多,如一人阅读,需要2,000小时才能完成。为加快审查新冠肺炎疫苗,卫生部为每个疫苗申报项目聘请了7到12名专家。他们的专长包括:毒性、传染病、临床药物、微生物和流行病学等。
专家小组的检查目标,是需要证实送检的疫苗不存在安全隐患。疫苗可在被接种的人的身体内产生充份的免疫反应,从而使得人避免感染。
沙玛说:「我们必须确定,疫苗的好处大过其可能的风险,以及这些疫苗是在一个持有牌照的地方生产的。该牌照的发放,必须达到规定和标准。」
她说,对于药厂的生产场地,不仅限于疫苗,也包括药品制造,卫生部和世界其他一些国家签署了互相认可的协议。双方互派人员去对方国家的药厂进行检查。「我们需要保证,双方的标准相同,程序相同。」
所有生产疫苗的地方,需要检查后发给牌照,之后还需经常检查,保证其环境达标。
检查内容包括产品(Product)─即该场地生产的药物;场地(Premises)─场地需要有特定的规格,比如特别的楼层,必须具备的通风系统;程序(Process)─生产该药品的一切程序;人(People)─在此间工作的人们需资格的认证。
加拿大接收24.9万支新冠疫苗!下周就到安省!
今天,加拿大总理杜鲁多宣布,加拿大会在12月份签收多达24.9万支疫苗。这批疫苗主要用于长期护理院的居民和在那里的工作人员。
虽然疫苗仍然在加拿大卫生部的批准之中,但杜鲁多表示,首批疫苗将在下周交付分发,而且其余批次将会在2021年陆续到达。
杜鲁多说:“我们正在面临着国家历史上最大规模的免疫接种。预计将要数月才能完成。”
“这不是一项小任务,因此我们有一个清晰的计划。我们的政府会通过国家操作中心,一直与各个省份和地区合作,以确保我们可以在批准和交付疫苗后,立即分发。”
与此同时,安省省长福特今早表示,加拿大接收的这批疫苗,最早将于下周在安省分发。福特说:“安省正在准备在疫苗到达后,立即分发这批非常少量的疫苗。”
“要让每一个人获得疫苗,任重而道远。我必须重申一次,我们距离实现大规模免疫所需的数百万支疫苗还很远。”
目前,加拿大已经与辉瑞公司签署了2000万支疫苗的订购协议,首批400万支疫苗将在2021年前3个月送达。该协议还允许加拿大有选择权,继续购买额外5600万支疫苗。辉瑞疫苗需要接种2支才能有效。
加拿大卫生部对辉瑞疫苗的审查正在进行,但是很快就会完成。卫生部首席医学顾问Dr. Supriya Sharma表示,她的部门可能最早在本周就会批准辉瑞疫苗。该时间表与美国监管机构的疫苗批准计划大致相同。
昨天,辉瑞疫苗的合作方德国BioNTech公司的首席业务和商务官Sean Marett表示:“我们已经准备好疫苗,一旦加拿大批准,24小时内就可以发货!”
同时,加拿大公共卫生局(PHAC)的物流和运营副总监(VP)Dany Fortin少将说:“我们预计,在明年1月份会有源源不断的疫苗,包括辉瑞疫苗和其他可用疫苗。然后,它们将会在规定的时间范围内,被一波接着一波地分发。”
Fortin少将对记者表示,他的计划是基于在新年之初收到疫苗的期望。“我目前能告诉你的是,我们希望在1月份收到疫苗,并且我们希望在那个时间范围内尽快收到它们,并且能够连续多次交付。”
他说:“我们的计划会从1月份开始执行。对我们而言,临近这个日期才开始准备,并不是一个明智的军事计划。因此,我们其实在12月中旬就会准备就绪。”
也就是说,就算是现在疫苗提前来了,加拿大也能立即行动!不过,近期有民调显示,有相当一部分的加拿大人表示他们将完全拒绝接种新冠疫苗,或者是等待一段时间后再接种。杜鲁多说,他希望加拿大人可以放心,加拿大的监管机构只会批准有效的产品,不会急于求成。
加拿大疫苗一点都不晚!和美国一样,仅次于英国。
Moderna公司创始人和主席Noubar Afeyan上周日接受加拿大CBC采访时称, 加拿大在获分配疫苗方面并不落后。
Moderna公司生产的新冠病毒疫苗 , 据说有效率可达94.5% 。
Noubar Afeyan称,这是因为加拿大是预订Moderna新冠疫苗的首批国家。
所以加拿大可以保证获得该公司的第一批(initial batch)出产疫苗的一部分。
Afeyan称,那些在疫苗效果还不知道的时候,就出钱的人,肯定可以获得相应的份额(出钱多少就分多少)。
Afeyan表示,不管后面发生什么,也改变不了这个事实。
高盛:加拿大和美国在明年4月前将有50%的人接种疫苗
另据高盛的最新预计,英国在明年3月之前将有50%的人接种疫苗,加拿大和美国在明年4月前将有50%的人接种疫苗
欧盟、澳大利亚和日本的接种人数可能会在5月份达到50% 。
民调指75%多市市民愿意接种新冠疫苗(图)

据多伦多市公共卫生局委托Ipsos Reid公司所做的民意调查显示,有75%的市民愿意接种新冠疫苗,超过世卫达到全民免疫的比例要求。
调查亦指出,有40%表示一定会接种,有33%称则称可能会。
另外,16%的受访者则表示不会或可能不会接种疫苗。另外有11%表示不知道。
调查访问了1201名市民。
审批辉瑞疫苗采弹性处理 允药厂「滚动报告」省时间(图)

联邦卫生部正在审批辉瑞药厂等的疫苗,今次的审批过程增加了弹性。
加拿大联邦卫生部正在审批辉瑞药厂等的疫苗,今次的审批过程增加了弹性,允许药厂从试制阶段的一开始,就「滚动报告」各种数据,而不是惯常的在完成所有试验之后,再把全部数据、资料呈报。这样可节省许多时间。卫生部首席医学顾问沙玛(Supriya Shama)说,滚动报告的情况下,所有必须做的试验、所有必须报告的数据,一样都不可缺少。因此在节省时间的同时,并不影响疫苗的安全性和功效。
疫苗厂商的一次性呈交的报告有数千页之多,如一人阅读,需要2,000小时才能完成。为加快审查新冠肺炎疫苗,卫生部为每个疫苗申报项目聘请了7到12名专家。他们的专长包括:毒性、传染病、临床药物、微生物和流行病学等。
专家小组的检查目标,是需要证实送检的疫苗不存在安全隐患。疫苗可在被接种的人的身体内产生充份的免疫反应,从而使得人避免感染。
沙玛说:「我们必须确定,疫苗的好处大过其可能的风险,以及这些疫苗是在一个持有牌照的地方生产的。该牌照的发放,必须达到规定和标准。」
她说,对于药厂的生产场地,不仅限于疫苗,也包括药品制造,卫生部和世界其他一些国家签署了互相认可的协议。双方互派人员去对方国家的药厂进行检查。「我们需要保证,双方的标准相同,程序相同。」
所有生产疫苗的地方,需要检查后发给牌照,之后还需经常检查,保证其环境达标。
检查内容包括产品(Product)─即该场地生产的药物;场地(Premises)─场地需要有特定的规格,比如特别的楼层,必须具备的通风系统;程序(Process)─生产该药品的一切程序;人(People)─在此间工作的人们需资格的认证。
最后编辑: 2020-12-07



