- 首页
-
菜单
- 家园币
-
比特币
Financial Markets by TradingView
您正在使用一款已经过时的浏览器!部分功能不能正常使用。
- 主题发起人 confiture
- 发布时间 2020-02-03
更多选项
导出主题(文本)这个药物现在由中日友好医院牵头在国内做三期试验,成为热点新闻。谈一点我的看法。
首先我希望这个药物能通过三期试验证明自己是治疗新冠病毒肺炎的特效药,这样对疫情的控制、对吉利德公司都是大利好。湖北省的新冠肺炎病死率远高于其他地方,我觉得是因为大量病人发病,超过了当地医疗系统的治疗能力,所以很多病人没有得到治疗所致。这个时候如果能有特效药物,那么可以大大缓解当地医疗系统的压力,也能救活更多的病人。
但是,这个药物是否有效还存疑,不宜现在就宣传为特效药。美国的第一例病人好转不能说明问题,因为很多因素不能排除,比如是否有其他药物的作用,病人是否病情较轻,甚至是特例等等。另外,三期临床试验的目的在验证药物是否有效的同时,还要观察药物的毒副作用,不少试验药物就是因为毒副作用太多或者太强而被淘汰。也就是说,即使一个药物非常有效,但是如果其毒副作用太强,这个药物在临床上等同于无效。所以现在说remdesivir是特效药还为时过早。
这次吉利德在中国进行三期临床试验从商业上说是个非常高明的操作。remdesivir本身设计是治疗ebola和马尔堡病毒感染,但是去年刚果卫生部宣布在治疗Ebola感染上,remdesivir和单克隆抗体相比并没有显示出更为有效。根据以前的统计,一个药物从实验室到获得FDA批准,平均要花费数以十亿记美元的研发成本。因此如过remdesivir不能通过三期临床,前期吉利德的大笔资金就打了水漂。如果此时能证明它能治疗新冠病毒肺炎,那么这个药物就起死回生了,吉利德前期的投资不仅被挽回还有可能大赚。而且最妙的是,三期临床试验的费用可能也免去了大部分。
吉利德公司本身是个技术水平非常高的公司,但是它的定价策略是高质高价,比如它的王牌药物,口服就可以完全治愈丙肝的三种产品,定价都在每疗程7.4万-8.5万美元。吉利德这次只是说提供一小批药物做三期临床试验,但是并没有承诺免费赠送专利或者授权中国药厂仿制,所以即使remdesivir被证实为特效药,也要看吉利德的定价策略是否还和以前一样,如果价格过高,那么对于中国病人来说能吃得起的也没几个。
最后网上的一些信息我不大相信。比如文学城的一条新闻
网爆美新药在中国进展极佳 病患24小时恢复(图)
第一,三期临床是严格的随机对照双盲试验。既然是双盲,那么无论受试的病人还是参加试验的医生,在试验结束开盲之前都不知道哪个病人用的是试验药物,哪个病人用的是安慰剂或者对照。这个新闻如果是真的,那么肯定有人违反了试验操作守则,也违反了试验伦理,严格来说会导致试验失效被取消。
第二,一般的三期临床,不会选取重症病人,只会选取轻症或者中等严重程度的病人。理由很简单,如果重症病人病死率高,那么可能会导致药物的效果被掩盖,对药厂是不利的。所以这个新闻里说重症病人很快好转,不符合一般的研究设计。
多么希望那些报道说成功救治,24小时生效是真的啊
这种时候真正应验了草民这两个字
吾心滴血ing
最近心情真是不好!
要是只有细胞培养和灵长动物实验,连临床一期,二期都没有,那这个药物的风险很大,效果更未必乐观
一个药如果没有三期临床,可能可以走FDA fast tracking 进入市场,以后补临床。。但没有一期,二期,上市应该不可能。。
治疗伊波拉,如果还不知道药代动力学,毒性,安全剂量,潜在副作用,谁敢直接上三期,用比较多人身上呢,非洲人也是人啊。。
这个药对于伊波拉病毒,是有动物,一期,二期实验的。。可以查得到。。三期因为没有做完,所以显示只做完了二期。。因为2018非洲伊波拉爆发,所以二期三期是有重叠的。关于三期的文章很多,就不给链接了。。
Remdesivir - Gilead Sciences - AdisInsight
Remdesivir (GS 5734) is a small molecule, monophosphoramidate prodrug of adenosine triphosphate analogue being developed by Gilead Sciences for the treatment of
我没有查证,但我觉得,如果一个药做完了一期二期,转去治疗另一个疾病或者适应症,在剂量剂型不变的情况下,特殊情况,是可以申请赦免,直接走三期的。。
一个药如果没有三期临床,可能可以走FDA fast tracking 进入市场,以后补临床。。但没有一期,二期,上市应该不可能。。
治疗伊波拉,如果还不知道药代动力学,毒性,安全剂量,潜在副作用,谁敢直接上三期,用比较多人身上呢,非洲人也是人啊。。
这个药对于伊波拉病毒,是有动物,一期,二期实验的。。可以查得到。。三期因为没有做完,所以显示只做完了二期。。因为2018非洲伊波拉爆发,所以二期三期是有重叠的。关于三期的文章很多,就不给链接了。。
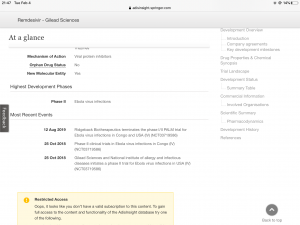
Remdesivir - Gilead Sciences - AdisInsight
Remdesivir (GS 5734) is a small molecule, monophosphoramidate prodrug of adenosine triphosphate analogue being developed by Gilead Sciences for the treatment ofadisinsight.springer.com
我没有查证,但我觉得,如果一个药做完了一期二期,转去治疗另一个疾病或者适应症,在剂量剂型不变的情况下,特殊情况,是可以申请赦免,直接走三期的。。
我觉得问题是换了个病毒,有效剂量是不是还是一样。如果剂量不一样,早期的一二期临床资料是不是全都能照搬过来,我不知道。
还有一个我觉得比较关键的是,大量轻中度病人并不需要什么特效药就能治好,所以现在的问题是对remdesivir的需要是不是那么迫在眉睫?现在还有大量的其他抗病毒药物可以用,前两天刚看到泰国医生用奥斯他韦联合一种抗艾滋病毒药物治疗新冠肺炎,据说也是有奇效。而对remdesivir疗效的期待多半来自于分析而不是实效。这种情况以前遇到过很多了,早期期望很高的试验药物最后在临床上一败涂地的事一点都不稀奇。
这个时候我觉得该做的临床试验还是要做,即使跳过一二期,三期临床也应该按照GCP标准一丝不苟的进行。而且我觉得应该在重病人里做试验,现在的主要问题是危重病人得不到救治,如果有特效药,能大大缓解临床对呼吸机和ECMO的需求。
行家一出手,就知有没有。这个药物现在由中日友好医院牵头在国内做三期试验,成为热点新闻。谈一点我的看法。
首先我希望这个药物能通过三期试验证明自己是治疗新冠病毒肺炎的特效药,这样对疫情的控制、对吉利德公司都是大利好。湖北省的新冠肺炎病死率远高于其他地方,我觉得是因为大量病人发病,超过了当地医疗系统的治疗能力,所以很多病人没有得到治疗所致。这个时候如果能有特效药物,那么可以大大缓解当地医疗系统的压力,也能救活更多的病人。
但是,这个药物是否有效还存疑,不宜现在就宣传为特效药。美国的第一例病人好转不能说明问题,因为很多因素不能排除,比如是否有其他药物的作用,病人是否病情较轻,甚至是特例等等。另外,三期临床试验的目的在验证药物是否有效的同时,还要观察药物的毒副作用,不少试验药物就是因为毒副作用太多或者太强而被淘汰。也就是说,即使一个药物非常有效,但是如果其毒副作用太强,这个药物在临床上等同于无效。所以现在说remdesivir是特效药还为时过早。
这次吉利德在中国进行三期临床试验从商业上说是个非常高明的操作。remdesivir本身设计是治疗ebola和马尔堡病毒感染,但是去年刚果卫生部宣布在治疗Ebola感染上,remdesivir和单克隆抗体相比并没有显示出更为有效。根据以前的统计,一个药物从实验室到获得FDA批准,平均要花费数以十亿记美元的研发成本。因此如过remdesivir不能通过三期临床,前期吉利德的大笔资金就打了水漂。如果此时能证明它能治疗新冠病毒肺炎,那么这个药物就起死回生了,吉利德前期的投资不仅被挽回还有可能大赚。而且最妙的是,三期临床试验的费用可能也免去了大部分。
吉利德公司本身是个技术水平非常高的公司,但是它的定价策略是高质高价,比如它的王牌药物,口服就可以完全治愈丙肝的三种产品,定价都在每疗程7.4万-8.5万美元。吉利德这次只是说提供一小批药物做三期临床试验,但是并没有承诺免费赠送专利或者授权中国药厂仿制,所以即使remdesivir被证实为特效药,也要看吉利德的定价策略是否还和以前一样,如果价格过高,那么对于中国病人来说能吃得起的也没几个。
最后网上的一些信息我不大相信。比如文学城的一条新闻
网爆美新药在中国进展极佳 病患24小时恢复(图)
第一,三期临床是严格的随机对照双盲试验。既然是双盲,那么无论受试的病人还是参加试验的医生,在试验结束开盲之前都不知道哪个病人用的是试验药物,哪个病人用的是安慰剂或者对照。这个新闻如果是真的,那么肯定有人违反了试验操作守则,也违反了试验伦理,严格来说会导致试验失效被取消。
第二,一般的三期临床,不会选取重症病人,只会选取轻症或者中等严重程度的病人。理由很简单,如果重症病人病死率高,那么可能会导致药物的效果被掩盖,对药厂是不利的。所以这个新闻里说重症病人很快好转,不符合一般的研究设计。
特讨厌一帮子啥都不懂的瞎BB。
小芳好文,不过说到你最后一段,“如果一个药做完了一期二期,转去治疗另一个疾病或者适应症,在剂量剂型不变的情况下,特殊情况,是可以申请赦免,直接走三期的”,本大王支持下面熊猫医生的观点,即使跳过临床一期,二期,该做的实验还是要做,临床三期也必须严格执行下去
因为现在病人太多,最怕就是这个药有一定效果,但有严重长期毒副作用(如同当年的反应停),仓促间大量病人用上,造成严重后果
因为现在病人太多,最怕就是这个药有一定效果,但有严重长期毒副作用(如同当年的反应停),仓促间大量病人用上,造成严重后果
一个药如果没有三期临床,可能可以走FDA fast tracking 进入市场,以后补临床。。但没有一期,二期,上市应该不可能。。
治疗伊波拉,如果还不知道药代动力学,毒性,安全剂量,潜在副作用,谁敢直接上三期,用比较多人身上呢,非洲人也是人啊。。
这个药对于伊波拉病毒,是有动物,一期,二期实验的。。可以查得到。。三期因为没有做完,所以显示只做完了二期。。因为2018非洲伊波拉爆发,所以二期三期是有重叠的。关于三期的文章很多,就不给链接了。。
Remdesivir - Gilead Sciences - AdisInsight
Remdesivir (GS 5734) is a small molecule, monophosphoramidate prodrug of adenosine triphosphate analogue being developed by Gilead Sciences for the treatment ofadisinsight.springer.com
我没有查证,但我觉得,如果一个药做完了一期二期,转去治疗另一个疾病或者适应症,在剂量剂型不变的情况下,特殊情况,是可以申请赦免,直接走三期的。。
Not necessarily. The most common approach is pharmacovigilance surveillance.长期毒付作用需要做四期实验才能知道,做3期实验,如果有很多的sae.或死亡,并且是和实验药物有关的,才会停,很少的情况
BTW, phase 3 RDV for 2019-hCoV study has been formally listed on clinicaltrials.gov. Check it out if you guys are interested. And interesting enough, it is not a Gilead study. The sponsor is listed as Capital Medical University. It is basically an IIR (independent investigative research), which means the commercializations pathway at this point is still uncertain.
Similar threads
- 2
家园推荐黄页
家园币系统数据
- 家园币池子报价
- 0.0097加元
- 家园币最新成交价
- 0.0101加元
- 家园币总发行量
- 1106666家园币
- 加元现金总量
- 12155.9加元
- 家园币总成交量
- 4098206.67家园币
- 家园币总成交价值
- 384692.02加元
- 池子家园币总量
- 396336.11家园币
- 池子加元现金总量
- 3850.24加元
- 池子币总量
- 35214.19
- 1池子币现价
- 0.2187加元
- 池子家园币总手续费
- 5731.58JYB
- 池子加元总手续费
- 595.28加元
- 入池家园币年化收益率
- 0.38%
- 入池加元年化收益率
- 4.08%
- 微比特币最新报价
- 0.135117加元
- 毫以太币最新报价
- 4.59786加元
- 微比特币总量
- 0.354108BTC
- 毫以太币总量
- 0.219250ETH
- 家园币储备总净值
- 531,531.68加元
- 家园币比特币储备
- 3.4200BTC
- 家园币以太币储备
- 15.1ETH
- 比特币的加元报价
- 135,117.30加元
- 以太币的加元报价
- 4,597.86加元
- USDT的加元报价
- 1.40325加元
- 交易币种/月度交易量
- 手续费
- 家园币
- 0.1%(0.01%-1%)
- 加元交易对(比特币等)
- 1%-2%
- USDT交易对(比特币等)
- 0.1%-0.6%